 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
分别往铜-锌原电池中的铜半电池或锌半电池中加入氨水,原电池电动势怎样变化?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“分别往铜-锌原电池中的铜半电池或锌半电池中加入氨水,原电池电…”相关的问题
更多“分别往铜-锌原电池中的铜半电池或锌半电池中加入氨水,原电池电…”相关的问题
第3题
A.原电池电动势减小
B.原电池电动势不变
C.原电油电动势增大
D.无法确定
第4题
已知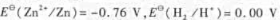 ,用两个电极组成原电池,电池符号为
,用两个电极组成原电池,电池符号为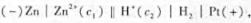 ,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的
,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的 。
。
第5题
欲使铜-锌原电池 的电动势增加,可以采取的措施有()。
的电动势增加,可以采取的措施有()。
A.增加锌离子的浓度
B.增加铜离子的浓度
C.减少铜离子的浓度
D.增加电极的尺寸
第7题
有一原电池,其电池符号为
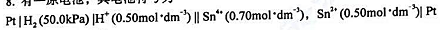
(1)写出半电池反应。
(2)写出电池反应。
(3)计算原电池的电动势。
(4)当E=0时,在保持p(H2)和c(H+)不变的情况下,c(Sn2+)/c(Sn4+)等于多少?
第9题
在标准态下将反应 ,改写成
,改写成 ,
, 下列说法中不正确的是()。
下列说法中不正确的是()。
A.电子得失数不间
B.组成原电池后,电池的电动势相同
C.反应的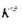 不同
不同
D.组成原电池后,铜作原电池的正极
第10题
已知下列原电池:
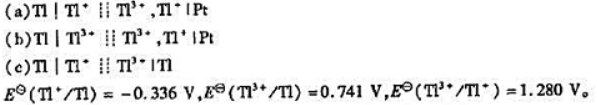
(1)写出各电池反应,并分别指出反应方程式中转移的电子数z;
(2)计算各电池的标准电动势EθMP;
(3)计算各电池反应的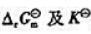 .
.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧