题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知,用两个电极组成原电池,电池符号为,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势
已知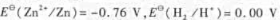 ,用两个电极组成原电池,电池符号为
,用两个电极组成原电池,电池符号为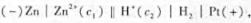 ,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的
,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的 。
。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


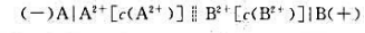 当c(A2+)=c(B2+)时,原电池的电动势为0.78V。现使上述原电池的电动势减小到原来的1/2,求此时两个电极中A2+浓度与B2+浓度的比
当c(A2+)=c(B2+)时,原电池的电动势为0.78V。现使上述原电池的电动势减小到原来的1/2,求此时两个电极中A2+浓度与B2+浓度的比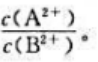
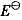 ,再计算电池反应的
,再计算电池反应的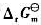 。
。
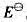 。
。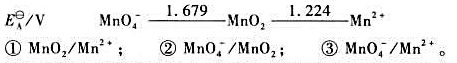
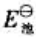 和电池反应的
和电池反应的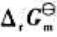 。
。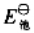 和电池反应的
和电池反应的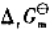 。
。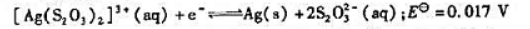
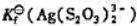 .
. ,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知
,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知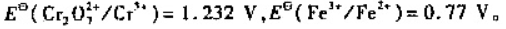

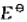 只取决于组成电池的两个电极,而与电池中各物质的浓度无关。()此题为判断题(对,错)。
只取决于组成电池的两个电极,而与电池中各物质的浓度无关。()此题为判断题(对,错)。