 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
把氧化还原反应Zn + 2Ag+ =Zn2+ + 2Ag 组成原电池,欲使该原电池的电动势增大,可采取的措施是()。
A.降低Zn2+浓度
B.降低Ag+浓度
C.增加Zn2+浓度
D.加大Ag电极的表面积
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.降低Zn2+浓度
B.降低Ag+浓度
C.增加Zn2+浓度
D.加大Ag电极的表面积
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“把氧化还原反应Zn + 2Ag+ =Zn2+ + 2Ag 组…”相关的问题
更多“把氧化还原反应Zn + 2Ag+ =Zn2+ + 2Ag 组…”相关的问题
第2题
将氧化还原反应 设计成原电池.该原电池的正极反应为().负极反应为()
设计成原电池.该原电池的正极反应为().负极反应为()
第3题
已知298.15K时,

(1)在298.15K时,把电对MnO2/Mn和CI2/CI-组成原电池,计算原电池的标准电动势;
(2)在298.15K时,计算当H+浓度为0.10mol·L-1、其他离子浓度均为1.0mol·L-1和Cl2分压为100kPa时原电池的电动势;
(3)计算298.15K时该原电池所对应的氧化还原反应的标准平衡常数。
第4题
A.电极反应中,增加氧化态物质的浓度。原电池的电动势降低
B. 代数值较小的电对的氧化态物质也有可能轧化
代数值较小的电对的氧化态物质也有可能轧化 代数值较大的电对中的还原态物质
代数值较大的电对中的还原态物质
C.原电池的电动势越大,电池反应的反应速率越快
D.氧化还原反应进行的方向是氧化能力较强的氧化型物质氧化还原能力较弱的还原型物质
第7题
已知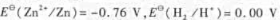 ,用两个电极组成原电池,电池符号为
,用两个电极组成原电池,电池符号为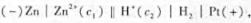 ,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的
,在298. 15K,原电池:的电动势为0.50 V,锌电极的电极电势为-0.80 V, 则锌电极中锌离子的浓度c1=()Mol· L-1,氢电极的电极电势E(H2/H+)=()。 氢半电池中氢离子的浓度c2=()mol· L-1,氢半电池中溶液的pH=().该氧化还原反应达到平衡时,反应的 。
。
第8题
欲使铜-锌原电池 的电动势增加,可以采取的措施有()。
的电动势增加,可以采取的措施有()。
A.增加锌离子的浓度
B.增加铜离子的浓度
C.减少铜离子的浓度
D.增加电极的尺寸
第9题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧