题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应N2O4(g)=2NO2(g)在60℃时=1.33.试求在60℃总压为100kPa的条件下:(1)纯N2O≇
反应N2O4(g)=2NO2(g)在60℃时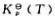 =1.33.试求在60℃总压为100kPa的条件下:
=1.33.试求在60℃总压为100kPa的条件下:
(1)纯N2O4(g)气体的解离度?
(2)1molN2O4(g)气体与2mol惰性气体的混合气中.N2O3(g)的解离度.与(l)比较,平衡向何方移动?
(3)当反应系统的总压为1000kPa时,N2O4的解离度又为若干?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


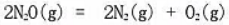 起始时N2O的压力为2.93X104Pa,并测得反应过程中系统的总压变化如下表所示:求最初300s与最后2000s的时间间隔内的平均速率。
起始时N2O的压力为2.93X104Pa,并测得反应过程中系统的总压变化如下表所示:求最初300s与最后2000s的时间间隔内的平均速率。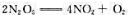 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算: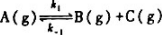 中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求:
中,k1和k-1,在25℃时分别为0.2s-1和.3.9477x10-3MPa-1.s-1.在35℃时二者皆增为2倍.试求: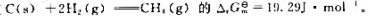 当总压为100kPa时,气相组成为70%H2、20%CH2和10%N2的条件下.该反应().
当总压为100kPa时,气相组成为70%H2、20%CH2和10%N2的条件下.该反应().
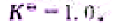
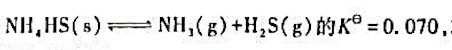 求:
求: