 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


294.8 K时,反应 求:(1)平衡时该气体混合物的总压;(2)在同样的实验中,NH3的最初分压为25.3 kPa
294.8 K时,反应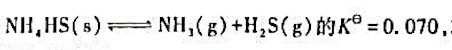 求:
求:
(1)平衡时该气体混合物的总压;
(2)在同样的实验中,NH3的最初分压为25.3 kPa时,H2S的平衡分压为多少?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


294.8 K时,反应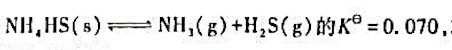 求:
求:
(1)平衡时该气体混合物的总压;
(2)在同样的实验中,NH3的最初分压为25.3 kPa时,H2S的平衡分压为多少?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“294.8 K时,反应 求:(1)平衡时该气体混合物的总压;…”相关的问题
更多“294.8 K时,反应 求:(1)平衡时该气体混合物的总压;…”相关的问题
第1题
反应N2O4(g)=2NO2(g)在60℃时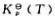 =1.33.试求在60℃总压为100kPa的条件下:
=1.33.试求在60℃总压为100kPa的条件下:
(1)纯N2O4(g)气体的解离度?
(2)1molN2O4(g)气体与2mol惰性气体的混合气中.N2O3(g)的解离度.与(l)比较,平衡向何方移动?
(3)当反应系统的总压为1000kPa时,N2O4的解离度又为若干?
第2题
某温度下,将一定瓜周体NHI4HS置于一真空容器中,它将按下式分解:
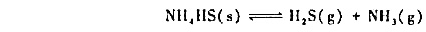
平衡时总I为68.0kPa。
(1)计算该分解反应的Kθ;
(2)保持温度不变,缓缓加入NH3直至NH3的平衡分压为93.0kPa,则此时H2S分正是多少?体系的总压是多少?
第3题
为40.0kPa的H2S,平衡后测得系统总压为77.8kPa;同样条件下,若将NH4HS(s)换成NH4Cl(s),平衡后测得系统总压为50.6kPa.试求:
(1)298K下两个分解反应的标准平衡常数和分解压力.
(2)298K下,将过量NH4HS(s)和NH4CI(s)同时置于抽空密闭容器中,达平衡时反应系统的总压.假设这两种盐类不形成固溶体.
第4题
3
:81/2H2O,其中NH3的蒸气分压为3.60kPa。试求:(1)从大量溶液(1)中转移lmolNH,至大量溶液(2)中,△G=?
(2)将压力为101.325kPa的lmolNH(g)溶解在大量溶液(2)中,AG=?
第5题
反应
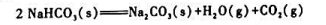
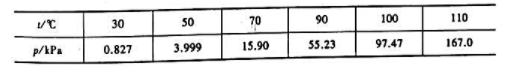
在不同温度时的平衡总压如下:
设反应的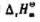 与温度无关.求:
与温度无关.求:
(1)上述反应的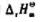 ;
;
(2)lg(p/kPa)与T的函敷关系式;
(3)NaHCO3的分解温度.
第6题
第7题
在308K和总压1.013x105Pa,N2O4有27.2%分解为NO2。
(1)计算 反应的
反应的 ;
;
(2)计算308K时总压为2.026x105Pa时,N2O4的离解百分率;
(3)从计算结果说明压强对平衡移动的影响。
第8题
1073K时,在密闭容器中进行如下可逆反应:

反应的标准平衡常数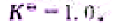
(1)如果反应开始时CO和H2O的分压都是100kPa,计算CO的平衡转化率;
(2)如果反应开始时CO的分压为100kPa,H2O的分压为500kPa,计算CO的平衡转化率。
第9题
第10题
已知反应:

298K时的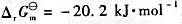 。试计算:
。试计算:
(1)该反应的标准平衡常数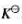 ;
;
(2)若空气中H2S的分压为3.1Pa,试计算可以确保铜单质免遭H2S腐蚀时H2的分压。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧