 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
计算 时Zn2+/Zn电对的条件电势。若,体系的电势是多少?
计算 时Zn2+/Zn电对的条件电势。若
时Zn2+/Zn电对的条件电势。若 ,体系的电势是多少?
,体系的电势是多少?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算 时Zn2+/Zn电对的条件电势。若
时Zn2+/Zn电对的条件电势。若 ,体系的电势是多少?
,体系的电势是多少?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“计算 时Zn2+/Zn电对的条件电势。若,体系的电势是多少?”相关的问题
更多“计算 时Zn2+/Zn电对的条件电势。若,体系的电势是多少?”相关的问题
第1题
己知pH=3.0时,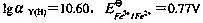 )
)
第3题
度为1.0×10mol·L-5,铁电对的电势是多少?共存的Fe(Ⅲ) 对测定有无干扰?若加入EDTA并使其过量的浓度为0.10mol·L-1,问此条件下, 铁电对的条件电势是多少?Fe(III) 的干扰能否被消除?
第4题
已知在酸性介质中,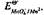 =1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
=1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
第5题
计算 的0.100mol·L-1氨溶液中Zn(NH3)42+/Zn电对的电势.
的0.100mol·L-1氨溶液中Zn(NH3)42+/Zn电对的电势.
第6题
用能斯特方程计算电对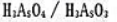 在pH=0,2,4,6,8,9时的电极电势,用计算的结果绘制pH-电势图,并用该图判断反应
在pH=0,2,4,6,8,9时的电极电势,用计算的结果绘制pH-电势图,并用该图判断反应

第8题
第9题
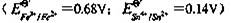
第10题
将电对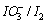 和
和 电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的
电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的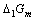 。
。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧