 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在酸性介质中,=1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推
已知在酸性介质中,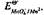 =1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
=1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在酸性介质中,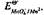 =1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
=1.45V,MnO4-被还原至一半时,体系的电势(半还原电位)为多少?试推出对称电对的半还原电势与其条件电势间的关系.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知在酸性介质中,=1.45V,MnO4-被还原至一半时,体…”相关的问题
更多“已知在酸性介质中,=1.45V,MnO4-被还原至一半时,体…”相关的问题
第1题
根据铬在酸性介质中的电势图:
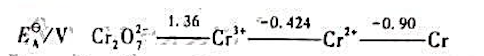
(1)计算 (2)判断Cr3+、Cr2+在酸性介质中是否稳定。
(2)判断Cr3+、Cr2+在酸性介质中是否稳定。
第3题
已知以下标准电极电势:

①画出酸性介质中铀的元素电势图;
②预测哪个氧化态最稳定;
③预测哪些氧化态会发生歧化反应;
④哪些氧化态在空气中不稳定?
第5题
如图所示,已知:
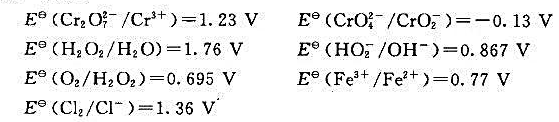
(1)试指出在酸性介质中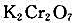 能氧化上面给出的哪些物质,并写出相关反应方程式。
能氧化上面给出的哪些物质,并写出相关反应方程式。
(2)欲使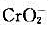 在碱性介质中被氧化,试指出上面给出的哪种氧化剂为好,并写出相关反应方程式。
在碱性介质中被氧化,试指出上面给出的哪种氧化剂为好,并写出相关反应方程式。
(3)试通过计算说明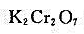 能否氧化浓度分别为
能否氧化浓度分别为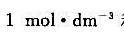 和
和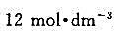 盐酸中的CI-。
盐酸中的CI-。
第7题
锰元素在酸性介质中的元素标准电极电势图为
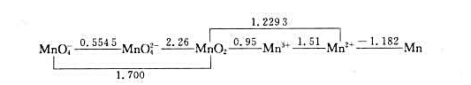
(1)试判断哪些物质可以发生歧化反应?写出歧化反应式;
(2)估计在酸性介质中,哪些物质是比较稳定的?
(3)试计算在酸性介质中电对MnO/Mn2+的标准电极电势。
第8题
试根据汞的元素电势图回答问题:
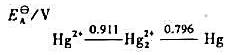
①在酸性介质中Hg22+能否发生歧化反应?
②计算反应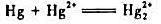 的平衡常数Kθ;
的平衡常数Kθ;
③拟使Hg(I)歧化为Hg(II)和Hg,应该怎样做?试举两个实例加以说明。
第9题
下列体系电位滴定至化学计量点时的电池电动势(用SCE作负极)为多少?
(a)在1mol·L-1HCL介质中,用Ce4+滴定Sn2+;
(b)在1mol·L-1H2SO4介质中,用Fe3+滴定UIV;
(c)在lmol·L-1H2SO4介质中,用Ce4+滴定vo2+.
第10题
试说明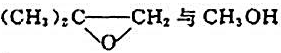 在酸性和碱性(CH3ONa)介质中反应生成两种不同异构体的原因。
在酸性和碱性(CH3ONa)介质中反应生成两种不同异构体的原因。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧