 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催
反应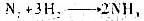 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应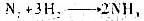 ,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
,在温度为773K.不使用做催化剂时反应的活化能为326.4kJ·mol-1,相同温度下使用Fe非催化剂.反应的活化能降为176kJ·mol-1.试计算此温度下两种反应速率之比。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“反应,在温度为773K.不使用做催化剂时反应的活化能为326…”相关的问题
更多“反应,在温度为773K.不使用做催化剂时反应的活化能为326…”相关的问题
第1题
反应 当反应在一定温度下达到化学平衡后,下列说法正确的是().
当反应在一定温度下达到化学平衡后,下列说法正确的是().
A、升高温度可使化学平衡向正反应方向移动
B、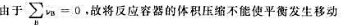
C、反应物的分压等于生成物的分压
D、加入催化剂,可使化学平衡向正反应方向移动
第2题
第3题
某对行反应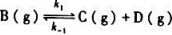 在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能
在300K时,k1=10s-1,k-1,=100Pa-1.s-1.当温度升高10°C时k1与k-1均增大一倍,则正、逆反应的活化能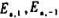 及反应的
及反应的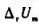 为().
为().
A.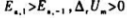
B.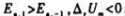
C.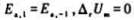
D.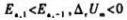
第5题
反应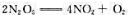 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
第7题
初始浓度开始,并都达到相同的转化率,两次实验所笛的时问分别为T1和T2.若反应为一级反应时所求得的活化能为En.1,反应为二级反应时所求得的活化能为En.2o则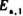 ()
()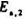 .
.
A.大于
B.等于
C.小于
D.既可能大于,也可能小于
第9题
应在323.15K温度下的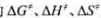 。
。

第10题
反应 在某温度下达到平衡。
在某温度下达到平衡。
(1)若其他条件不变,加入催化剂是否会引起平衡移动?
(2)若增大任一反应物或生成物的分压,化学平衡向哪一方向移动?
(3)升高温度时标准平衡常数是否发生变化?化学平衡向哪一方向移动?
(4)缩小容器的体积增大压力时,化学平衡向哪一方向移动?标准平衡常数是否发生变化?


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧