 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
I2在水中的溶解度很小,试从下列两个半反应计算在298K时,I2饱和溶液的浓度。(2)将0.100
I2在水中的溶解度很小,试从下列两个半反应计算在298K时,I2饱和溶液的浓度。
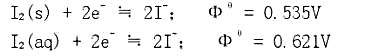
(2)将0.100mol I2溶解在1.00L 0.100mol.L-1KI溶液中而得到I3-溶液。I3-生成反应的Kc值为0.752,求I3-溶液中I2的浓度。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
I2在水中的溶解度很小,试从下列两个半反应计算在298K时,I2饱和溶液的浓度。
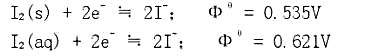
(2)将0.100mol I2溶解在1.00L 0.100mol.L-1KI溶液中而得到I3-溶液。I3-生成反应的Kc值为0.752,求I3-溶液中I2的浓度。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“I2在水中的溶解度很小,试从下列两个半反应计算在298K时,…”相关的问题
更多“I2在水中的溶解度很小,试从下列两个半反应计算在298K时,…”相关的问题
第1题
已知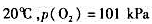 时,氧气在水中溶解度为1.38x10-3mol/L
时,氧气在水中溶解度为1.38x10-3mol/L
①写出反应 的标准平衡常数表达式,并计算在20℃时的
的标准平衡常数表达式,并计算在20℃时的 ;计算20℃时与101kPa大气平衡的水中氧的浓度C(O2),已知:大气中p(O2)=21.0kPa。
;计算20℃时与101kPa大气平衡的水中氧的浓度C(O2),已知:大气中p(O2)=21.0kPa。
②已知血红蛋白(Hb)氧化反应 在20℃时
在20℃时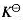 =85.5,计算反应
=85.5,计算反应 。
。
第2题
已知反应:
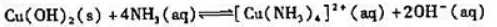
(1)计算该反应在298K下的标准平衡常数;
(2)估算Cu(OH)2在6.0mol·L-1氨水中的溶解度(mol·L-1)(忽略氨水浓度的变化).
第3题
第4题
298.15K时,Mg(OH)2的标准溶度积常数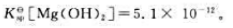 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
第5题
n(OH)2的饱和溶液中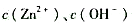 和pH;(3)Zn(OH)2在0.10mol/LNaOH中的溶解度;(4)Zn(OH)2在 0.10mo/LZnSO4中的溶解度。
和pH;(3)Zn(OH)2在0.10mol/LNaOH中的溶解度;(4)Zn(OH)2在 0.10mo/LZnSO4中的溶解度。
第6题
碘在水中溶解度很小,但在含有l-的溶液中的溶解度增大,这是因为发生了反应:
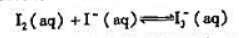
已经测得不同温度下的该反应的标准平衡常数结果见表4-1.

(1)画出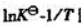 图;
图;
(2)估算该反应的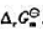 ;
;
(3)计算298K下该反应的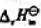 .
.
第7题
。
第8题
测得水层中含有0.233mmol的碘.计算碘在两分中的分配系数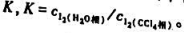 .设碘在两种溶剂中均以I2分子形式存在.
.设碘在两种溶剂中均以I2分子形式存在.
(2)若25℃I2在水中的浓度是1.33mmol.dm-3,求碘在CCl4中的浓度.
第9题
3)的ΔtGm(298K)为-16.78kJ·mol-1,则当p1=p2=p3=-1000kPa时,ΔtGm(298K)=().
第10题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧