 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知原电池: 的电动势为。 (1)试求; (2)若正极Cl2的压力为,Cl-离子的初始浓度为0
已知原电池:
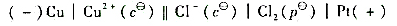
的电动势为 。
。
(1)试求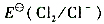 ;
;
(2)若正极Cl2的压力为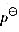 ,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知原电池:
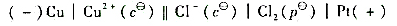
的电动势为 。
。
(1)试求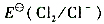 ;
;
(2)若正极Cl2的压力为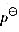 ,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
,Cl-离子的初始浓度为0.10moldm-3,负极Cu2+离子的初始浓度为0.010mol·dm-3,试求原电池的电动势E池。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知原电池: 的电动势为。 (1)试求; (2)若正极Cl2…”相关的问题
更多“已知原电池: 的电动势为。 (1)试求; (2)若正极Cl2…”相关的问题
第1题
已知298.15K时,

(1)在298.15K时,把电对MnO2/Mn和CI2/CI-组成原电池,计算原电池的标准电动势;
(2)在298.15K时,计算当H+浓度为0.10mol·L-1、其他离子浓度均为1.0mol·L-1和Cl2分压为100kPa时原电池的电动势;
(3)计算298.15K时该原电池所对应的氧化还原反应的标准平衡常数。
第2题
已知反应
2Cr3++3Cl2+7H2O=Cr2O72-+6C1-+14H+
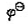 (Cr2O72-/Cr3+)=1.33V,
(Cr2O72-/Cr3+)=1.33V,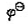 (Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(Cl2/CI-)=1.36V,F=95500J·V-1·mol-2若在298K时组成原电池。
(1)写出该原电监的电池符号,并计算标准电动势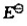 ;(2)计算
;(2)计算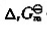 (298K)并判断反应进行的方向;(3)计算标准平衡常数
(298K)并判断反应进行的方向;(3)计算标准平衡常数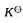 ;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
;(4)若c(H+)=10mol·dm-3,其他离子浓度均为标准浓度,求原电池的电动势E并判断反应进行的方向
第4题
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势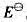 。
。
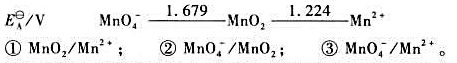
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势 和电池反应的
和电池反应的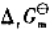 。
。
第5题
298K时,下列电池的电动势为1.228V:
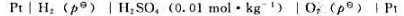
已知H2O(I)的标准生成焓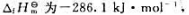 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
第6题
有一原电池,其电池符号为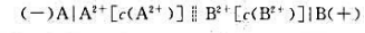 当c(A2+)=c(B2+)时,原电池的电动势为0.78V。现使上述原电池的电动势减小到原来的1/2,求此时两个电极中A2+浓度与B2+浓度的比
当c(A2+)=c(B2+)时,原电池的电动势为0.78V。现使上述原电池的电动势减小到原来的1/2,求此时两个电极中A2+浓度与B2+浓度的比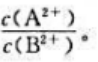
第7题
在pH=2,其他有关离子浓度为1.0 mol·L-1时,将电对 ,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知
,Fe1+/Fe2+组装成原电池,计算原电池的电动势,写出电极反应、电池反应。已知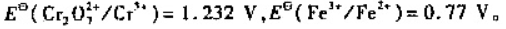
第8题
(1)试写出A和B组成的原电池的电池符号;
(2)试计算A和B组成的原电池的电动势;
(3)试求当A池中的c(Zn2+)消耗掉0.020mol·dm-3时,原电池的电动势。
第9题
已知如下两个原电池:

298.15K时,两个原电池的电动势分别为0.420V和0.334V,求胃液的pH。
第10题
已知随机变量X的概率密度函数为
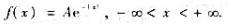
试求:(1)A;(2)P(0< χ< 1);(3)x的分布函数.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧