 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,下列电池的电动势为1.228V:已知H2O(I)的标准生成焓试求:(1)该电池的温度系数:(2)
298K时,下列电池的电动势为1.228V:
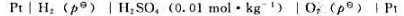
已知H2O(I)的标准生成焓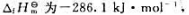 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,下列电池的电动势为1.228V:
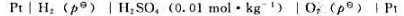
已知H2O(I)的标准生成焓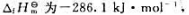 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“298K时,下列电池的电动势为1.228V:已知H2O(I)…”相关的问题
更多“298K时,下列电池的电动势为1.228V:已知H2O(I)…”相关的问题
第1题
请:
(1)写出电极反应及电池反应:
(2)求该电池反应的ΔtGmθ和电池在298K时的标准电动势:
(3)已知H2O(l)的生成热为-286.kJ·mol-1,试求该电池的温度系数;
(4)若在0~25℃范围内,电池反应的ΔtHm可看作常数,求0℃时该电池的电动势;
第2题
298K时,电池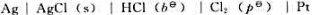 的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
的电动势为1.1362v,电动势的温度系数为-5.95X10-4V·K-1.
(1)写出电池反应;
(2)计算298K时该反应的 和标准平衡常数
和标准平衡常数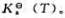
第3题
t(s)的电动势E=-1.228V,H2O(l)的标准生成焰为-285.5kJ·mol-1,请:
(1)写出电极反应及电池反应;
(2)求该电池的电动势温度系数;
(3)求电池反应的 ;
;
(4)求273K时电池的电动势(假设反应热ΔtHmθ在0~25C之间不随温度变化).
第4题
kJ.mol^-1。计算在氢氧燃料电池中进行下列反应时电池的电动势及其温度系数,

(2)应用表7.7.1的数据计算上述电池的电动势。
第5题
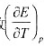
为1.40x10-4V/K。
第6题
电池Ag(s)AgCl(s)]KCl(m)|Hg2Cl2(s)|HIg(I)的电池反应为
Ag(s)+1/2Hg2CI2(s)→AgCl(s)+Hg(I),已知298K时,此电池反应的焓变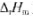 为5435/mol,各物质的规定熵数据为
为5435/mol,各物质的规定熵数据为
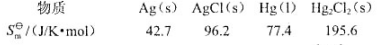 试计算该温度下电池的电动势E及电池电动势的温度系数
试计算该温度下电池的电动势E及电池电动势的温度系数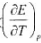
第7题
HCI的分压为46.4Pa.请:
(1) 试设计一电池以计算298K时HCI(g)分解为H2(g)和Cl2(g)的化学平衡常数.已知Eθ(CI-ICl2)
=1.360V;
(2)试求298K时该电池的电动势.
第8题
第9题
第10题
298K时,测得下列电池的电动势:
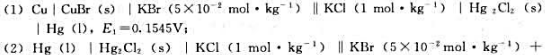
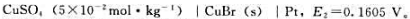
(3)如果忽略生成配合物的可能性和活度因子变化的影响,试计算下列电池的电动势


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧