 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
体系中开始有6mol的H2(g)和5mol的N2(g),反应一段时间后生成了2mol的NH3(g),此时的反应进度为()。
A.1mol
B.2mol
C.5mol
D.无法计算
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1mol
B.2mol
C.5mol
D.无法计算
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“体系中开始有6mol的H2(g)和5mol的N2(g),反应…”相关的问题
更多“体系中开始有6mol的H2(g)和5mol的N2(g),反应…”相关的问题
第1题
A.2mol/L盐酸、2mol/L铋酸钠
B.浓硝酸、1mol/L硝酸银
C.6mol/L硫酸、固体氯化钠
D.2mol/L硝酸、固体铋酸钠
第2题
第4题
第5题
第6题
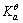 =1.8x10-5。
=1.8x10-5。
第7题
25.℃下,密闭恒容的容器中有10g固体萘(C10H8)在过量的O2中完全燃烧:
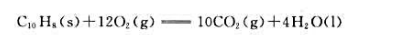
此反应过程放热401.73kJ,计算此时的反应进度及萘的完全燃烧反应的标准摩尔热力学能变和标准摩尔焓变。
第8题
第9题
PtCI4和氨水反应,生成物的分子式为 。用AgNO3处理lmol该化合物,得到2mol的AgCl。试推断该配合物的结构式并指出铂的配位数和配离子的化合价。
。用AgNO3处理lmol该化合物,得到2mol的AgCl。试推断该配合物的结构式并指出铂的配位数和配离子的化合价。
第10题
A.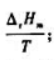
B.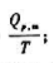
C.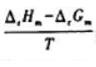
D.0


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧