 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
生产自来水时需通入Cl2杀菌消毒,主要是由于Cl2和H2O反应生成的HClO具有()
A.氧化性
B.酸性
C.还原性
D.稳定性
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.氧化性
B.酸性
C.还原性
D.稳定性
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“生产自来水时需通入Cl2杀菌消毒,主要是由于Cl2和H2O反…”相关的问题
更多“生产自来水时需通入Cl2杀菌消毒,主要是由于Cl2和H2O反…”相关的问题
第1题
已知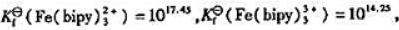 其他数据查附表.
其他数据查附表.
(1)计算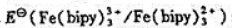 ;
;
(2)将Cl2(g)通入[Fe(bipy)3]2+溶液中,Cl2能否将其氧化?写出反应方程式,并计算25℃下该反应的标准平衡常数Kθ;
(3)若溶液中[Fe(bipy)3]2+的依度为0.20mol·L-1,所通Cl2的压力始终保持100.0KθPa,求平衡时溶液中各离子浓度.
第2题
(1)写出电池反应方程式;
(2)由附表六查得Eθ(Cl2/Cl-),计算E(Co2+/Co);
(3)p(Cl2)增大时,电池的电动势将如何变化?
(4)当CO2+浓度为0.010mol·L-1其他条件不变时,电池的电动势是多少伏?
第4题
A.臭氧的杀菌原理主要是靠强大的氧化作用,使酶失去活性导致微生物死亡
B.对空气中的微生物有明显地杀灭作用,可以除异味,净化环境,使空气清新
C.臭氧可与食品直接接触,用于食品消毒、保鲜,对食品不产生残余污染,不影响营养成份
D.用臭氧消毒空气,必须是在人不在的条件下,消毒后至少过30分钟才能进入
第6题
A.增大压力,使体积缩小
B.保持压力不变,通入惰气使体积增大
C.保持体积不变,通入惰气使压力增大
D.保持体积不变,通入Cl2气
第8题
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应: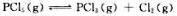 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数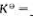 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
第11题
(1)将气体总压降低,直至体积为2dm3;
(2)总压保持在101.3kPa的条件下,通人N2,至体积变为2dm3;
(3)保持体积为1dm3的条件下,通入N2使压力增至202.6kPa;
(4)保持体积为1dm3的条件下,通入Cl2使压力增至202.6kPa;
(5)保持总压为101.3kPa的条件下,通入Cl2使体积增至2dm3.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧