 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在体积为V的立方形容器中有极大数目的三维平动子,其h2/(8mV2/3)=0.1kT,试计算该系统在平衡情况下,nx2+ny2+nz2=14的平动能级上粒子的分布数n与基态能级的分布数n0之比.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在体积为V的立方形容器中有极大数目的三维平动子,其h2/(8…”相关的问题
更多“在体积为V的立方形容器中有极大数目的三维平动子,其h2/(8…”相关的问题
第1题
在体积为V的立方形容器中有极大数月的三维平动子,其式
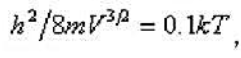
计算该系统在平衡情况下,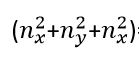 =14的平动能级上粒子的分布数n与基态能级的分布数n0之比。
=14的平动能级上粒子的分布数n与基态能级的分布数n0之比。
第2题
A.1
B.3
C.4
D.6
第3题
已知在立方容器中运动的三维平动子的能量计算公式:
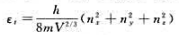
(1)求平动能级ε1=6h2/(8mV2/3)的多重度.
(2)室温下,在边长等于0.10m的立方容器中进行平动的H2分子,其平动能ε1=6.2X10-23,求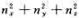 应为多少才与这个平动能相当?
应为多少才与这个平动能相当?
第4题
500K时,反应:
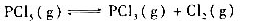
在一容积为1.00dm3的容器中进行。
(1)反应开始时容器内有0.010molPCl5,PCl5的平衡转化率为65.5%。试求该反应的Kr;
(2)反应开始时容器内有0.010molPCl5和0.010molPCl3,试求PCl5的平衡转化率;
(3)试求该温度下反应的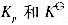 。
。
第5题
在500K时将 在体积为15.0L的容器内达到下列化学平衡:
在体积为15.0L的容器内达到下列化学平衡: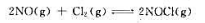 当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
第6题
1mol氧气,温度为300K时,体积为2.0X10-3m3。试计算;
(1)绝热膨胀至体积为20X1031m3,氧气所做的功;
(2)等温膨胀至体积为20X10-3m3,然后在保持体积不变情况下冷却,直到温度等于(1)中绝热膨胀后所达到的温度,此过程氧气做的功。
第7题
强从po降为p,活塞应往复运动多少次?设气体温度始终不变,(2)试利用(1)的结果证明排气管中气体压强和排气时间t的函数关系为
其中C称为排气速度(C=γ△V,γ为单位时间内活塞的往复次数)。
第9题
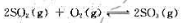
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
第10题
已知反应:

在45℃时,将0.0030mol的N2O.注入容积为0.50L的真空容器中,系统达平衡时,压力为26.3kPa,试计算:
(1)45℃时N2O4,的分解率及反应的标准平衡常数:
(2)25℃时反应的标准平衡常数;
(3)25℃时反应的标准摩尔熵变;
(4)反应的标准摩尔Cibbs函数变随温度变化的函数关系式.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧