 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件下通氢气使Fe2O3还原为F
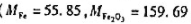
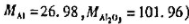
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
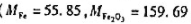
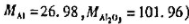
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件…”相关的问题
更多“称取纯Fe2O3和Al2O3混合物0.5622g,在加热条件…”相关的问题
第1题
称取铁样0.2801g,溶解后,将溶液中的Fe3+还原为Fe2+,然后用0.02000mol·L-1
K2Cr2O7标准溶液滴定,用去25.60mL,试计算:(1)K2Cr2O7标准溶液对Fe及(Fe2O3)滴定度;(2)试样中w(Fe)和w(Fe2O3).
第2题
第3题
准确称取铁矿石试样0.5000g,用酸溶解后加入SnCl2,使Fe3+还原为Fe2+,滴定Fe2+消耗24.50mLKMnO4标准溶液滴定,已知1mL.KMnO4相当于0.01260gH2C2O4·2H2O,(1)矿样中Fe及Fe2O3的质量分数各为多少?(2)取市售双氧水3.00mL,稀释定容于250.00mL,从中取出20.00mL试液,需用上述溶液KMnO421.18mL滴定至终点,计算每100.0mL市售双氧水所含H2O2的质量.
第4题
2
O3等杂质).将不纯的SiO2用H2SO4-HF.处理,使SiO2转化为SiF4而除去.残渣经灼烧后,其质量为0.0013g.计算试样中纯SiO2的含量.若不经H2SO4-HF处理,杂质造成的误差有多大?
第5题
,以磺基水杨酸为指示剂。用0.02000mol·L-1EDTA标准溶液滴定试样中的Fe3+。用去18.16ml.然后将试液调至pH=3.5,加入上述EDTA标准溶液25.0mL,并加热煮沸。再调试液pH=4.5.以PAN为指示剂,趁热用CuSO4标准溶液(每毫升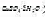 为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
为0.005000g)返滴定,用去8.12mL.计算试样中Fe2O3,和Al2O3,的质量分数。
第6题
第7题
试计算Fe2O3(s)+Al(s)-→Al2O3(s)+Fe(s)反应的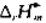 及
及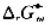 .在298K时,铝箔与Fe2O3有什么样的反应?为什么?实际上在298K时反应又是如何进行?
.在298K时,铝箔与Fe2O3有什么样的反应?为什么?实际上在298K时反应又是如何进行?
第8题
第9题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧