 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在200℃下体积为V的容器里,下面的吸热反应达成平衡态:通过以下各种措施,反应再达到平衡态时,NH3
在200℃下体积为V的容器里,下面的吸热反应达成平衡态:
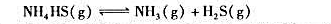
通过以下各种措施,反应再达到平衡态时,NH3的分压跟原来的分压相比,有何变化?
A.增加氨气
B.增加硫化氢气体
C.增加NH4HS固体
D.增加温度
E.加入氩气以增加体系的总压
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在200℃下体积为V的容器里,下面的吸热反应达成平衡态:
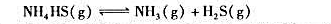
通过以下各种措施,反应再达到平衡态时,NH3的分压跟原来的分压相比,有何变化?
A.增加氨气
B.增加硫化氢气体
C.增加NH4HS固体
D.增加温度
E.加入氩气以增加体系的总压
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“在200℃下体积为V的容器里,下面的吸热反应达成平衡态:通过…”相关的问题
更多“在200℃下体积为V的容器里,下面的吸热反应达成平衡态:通过…”相关的问题
第1题
下面的反应在一个1L的容器里,在298K下达成平衡
C(石墨)+O2(g)=CO2(g)
以下各种措施对氧气的平衡分压有何影响?
A增加石墨的量。
B增加CO2气体的量。
C增加氧气的量。
D降低反应的温度。
E加入催化剂。
第2题
证明下列平衡判据(假设S>0);
(a)在s,V不变的情形下,稳定平衡态的U最小.
(b)在s,p不变的情形下,稳定平衡态的H最小.
(c)在H,p不变的情形下,稳定平衡态的s最小.
(d)在F,v不变的情形下,稳定平衡态的T最小.
(e)在G,p不变的情形下,稳定平衡态的T最小.
(f)在U,s不变的情形下,稳定平衡态的V最小.
(g)在F,T不变的情形下,稳定平衡态的V最小.
参考答案:为了判定在给定的外加约束条件下系统的某状态是否为稳定的平衡状态,设想系统围绕该状态发生各种可能的自发虚变动.由于不存在自发的可逆变动,根据热力学第二定律的数学表述(式(1.16.4)),在虚变动中必有
式中ꝽU和ꝽS是虛变动前后系统内能和熵的改变,dW是虛变动中外界所做的功,T是虚变动中与系统交换热量的热源温度.由于虚变动只涉及无穷小的变化,T也等于系统的温度.下面根据式(1)就各种外加约束条件导出相应的平衡判据.
(a) 在s,v不变的情形下,有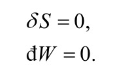
根据式(1),在虚变动中必有
如果系统达到了U为极小的状态,它的内能不可能再减少,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在S,V不变的情形下,稳定平衡态的U最小.
(b) 在s,p不变的情形下,有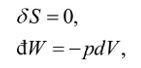
根据式(1),在虚变动中必有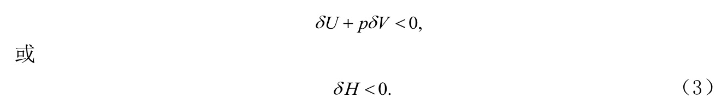
如果系统达到了H为极小的状态,它的焓不可能再减少,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在s,p不变的情形下,稳定平衡态的H最小.
(c) 根据焓的定义H=U+pV和式(1)知在虚变动中必有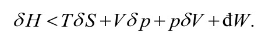
在H和p不变的的情形下,有
在虚变动中必有
如果系统达到了S为极大的状态,它的熵不可能再增加,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在H,p不变的情形下,稳定平衡态的S最大.
(d) 由自由能的定义F=U-TS和式(1)知在虚变动中必有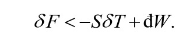
在F和V不变的情形下,有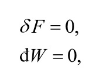
故在虚变动中必有
由于S>0,如果系统达到了T为极小的状态,它的温度不可能再降低,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在F,v不变的情形下,稳定平衡态的T最小
(e) 根据吉布斯函数的定义G=U-TS+pV和式(1)知在虚变动中必有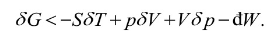
在G,p不变的情形下,有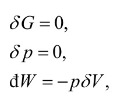
故在虚变动中必有
由于S>0,如果系统达到了T为极小的状态,它的温度不可能再降低,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在G,p不变的情形下,稳定的平衡态的T最小.
(f) 在U,S不变的情形下,根据式(1)知在虚变动中心有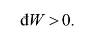
上式表明,在U,S不变的情形下系统发生任何的宏观变化时,外界必做功,即系统的体积必缩小,如果系统已经达到了V为最小的状态,体积不可能再缩小,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在U,S不变的情形下,稳定平衡态的V最小
(g) 根据自由能的定义F=U-TS和式(1)知在虚变动中必有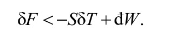
在F,T不变的情形下,有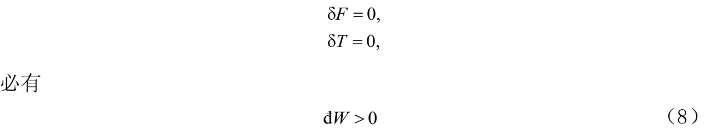
上式表明,在F,T不变的情形下,系统发生任何宏观的变化时,外界必做功,.即系统的体积必缩小.如果系统已经达到了V为最小的状态,体积不可能再缩小,系统就不可能自发发生任何宏观的变化而处在稳定的平衡状态,因此,在F,T不变的情形下,稳定平衡态的V最小.
1、证明下列平衡判据(假设S>0);
(a)在s,V不变的情形下,稳定平衡态的U最小.
(b)在s,p不变的情形下,稳定平衡态的H最小.
(c)在H,p不变的情形下,稳定平衡态的s最小.
(d)在F,v不变的情形下,稳定平衡态的T最小.
(e)在G,p不变的情形下,稳定平衡态的T最小.
(f)在U,s不变的情形下,稳定平衡态的V最小.
(g)在F,T不变的情形下,稳定平衡态的V最小.
第3题
在500K时将 在体积为15.0L的容器内达到下列化学平衡:
在体积为15.0L的容器内达到下列化学平衡: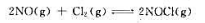 当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
第4题
五氧化二磷(PCI3)分解反应
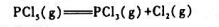
在200℃时的K°=0.312,计算:
(1)200℃,200kPa下PCI3的解离度;
(2)摩尔比为1:5的PCI3与CI2的混合物,在200℃,100kPa下达到平衡时PCI3的解高度.
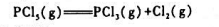
第5题
五氯化磷分解反应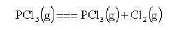 在200°C时的K=0.312,计算:
在200°C时的K=0.312,计算:
(1)200°C,200kPa下PCl5的解离度。
(2)摩尔比为1:5的PCl5与Cl2的混合物,在200°C,101.325kPa下,求达到化学平衡时PCl5的解离度。
第6题
已知25℃时,Mn(OH)2的溶度积为1.9x10-13,NH3·H2O的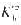 = 1.8×10-5,求:
= 1.8×10-5,求:
(1)25℃时,Mn(OH)2的溶解度;
(2) 在200 mL 0.2 mol·L-1MnCl2溶液中加入200 mL 0.2 mol·L-1NH3·H2O溶液和4.28 g NH4CI固体,有无沉淀生成?
第7题
第8题
第9题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧