 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有100m1Ca2+和Ba2+的混合溶液,两种离子的浓度都为0.010mo1·L-1(1)用Na2
现有100m1Ca2+和Ba2+的混合溶液,两种离子的浓度都为0.010mo1·L-1
(1)用Na2SO4作沉淀剂能否将Ca2+和Ba2+分离?
(2)加入多少克Na2SO4才能达到Ba2SO4全沉淀的要求(忽略加入Na2SO4引起的体积变化)?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有100m1Ca2+和Ba2+的混合溶液,两种离子的浓度都为0.010mo1·L-1
(1)用Na2SO4作沉淀剂能否将Ca2+和Ba2+分离?
(2)加入多少克Na2SO4才能达到Ba2SO4全沉淀的要求(忽略加入Na2SO4引起的体积变化)?
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“现有100m1Ca2+和Ba2+的混合溶液,两种离子的浓度都…”相关的问题
更多“现有100m1Ca2+和Ba2+的混合溶液,两种离子的浓度都…”相关的问题
第2题
计算(¿21¿)0.10mol/LH2CO3溶液中各离子浓度:(2)若用HCI调节pH=I.00时,溶液中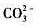 的浓度。(已知:
的浓度。(已知: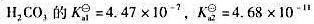 )
)
第3题
已知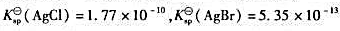 ,在含有等浓度的Br-和CI-的混合溶液中逐滴加入AgNO3溶液,哪种离子先沉淀()
,在含有等浓度的Br-和CI-的混合溶液中逐滴加入AgNO3溶液,哪种离子先沉淀()
A.Br-
B.CI-
C.同时沉淀
D.无法判断
第4题
A、

B、
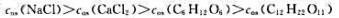
C、
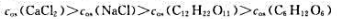
D、
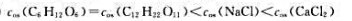
第5题
按下列体积比混合相同浓度的HAc和NaOH两种溶液,混合后溶液的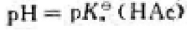 的是()。
的是()。
A、1:1
B、2:3
C、1:2
D、3:1
第6题
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
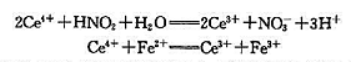
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.
第8题
第9题
第10题


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧