 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
解释下列事实:(1)MgO可作为耐火材料;(2)金属Al和Fe都能压成片、抽成丝,而石灰石则不能;(3)在卤化银中,AgF可溶于水,其余卤化银则难溶于水,且从AgCI到Agl溶解度诚小;(4)NaCl易溶于水,而CuCl难溶于水。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“解释下列事实:(1)MgO可作为耐火材料;(2)金属Al和F…”相关的问题
更多“解释下列事实:(1)MgO可作为耐火材料;(2)金属Al和F…”相关的问题
第1题
简要回答下列问题:
(1)为什么金属Fe与盐酸反应生成Fe(Ⅱ),而与氯气反应生成Fe(Ⅲ)?
(2)向Pb2+的溶液中加入稀盐酸,然后过滤,测得滤液中仍有较多Pb(Ⅱ)。试解释其原因。
(3)为什么卤素互化物中卤素原子的数目经常是偶数,而碱金属多卤化物中卤素原子的数目却经常是奇数?
(4)氢氟酸在较稀的溶液中是完全解离的,但实测的Ka却为10-4数量级,属于弱酸。应如何解释?而浓的氢氟酸,其酸性较强。又应如何解释?
(5)常温下测得卤化氢气体对空气的相对密度是
HF 1.78;HCl 1.26;HBr 2.79;H 14.44。
由此计算出卤化氢的相对分子质量,HCI,HBr,HI均接近理论值,唯HF的相对分子质量与理论值20相差很大,试说明其原因。
(6)HClO,HClO2,HClO3,HClO4的酸性依次增强,试说明其原因。
(7)HClO,HClO3,HClO4的氧化性依次减弱,试说明其原因。
第2题
第4题
298K下,分别将金属Fe和Cd插入下述溶液中组成电池,试判断何种金属首先被氧化?(所需数据可查表).
(1)溶液中含Fe2+和Cd2+的浓度都是0.1mol·kg-1.
(2)溶液中b(Fe2+)=0.1mol·kg-1,b(Cd2+)=0.0036mol·kg-1.
第8题
如何解释下列事实:
(1)锂的电离能比铯大,但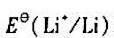 却比
却比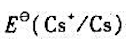 小;
小;
(2)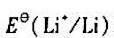 比
比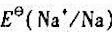 小,但锂同水的作用不如钠激烈;
小,但锂同水的作用不如钠激烈;
(3) LiI比KI易溶于水,而LiF比KF难溶于水;
(4) BeCl2 为共价化合物,而CaCl2为离子化合物;
(5)金属钙与盐酸反应剧烈,但与硫酸反应缓慢;
(6)消防队员的空气背包中放有KO2。
第9题
解释下列问题
钴(II)盐不稳定而其配离子稳定,钴(II)盐则相反;
(1)当Na2CO3溶液与FeCl3溶液反应时,为什么得到的是氢氧化铁而不是碳酸铁?
(2)为什么不能在水溶液中由Fe3+盐和KI制得FeI3?
(3)Fe与Cl2可得到FeCl3,而Fe”与HCl作用只得到FeCl3;
(4)Co和Ni的相对原子质量与原子序数的顺序为何相反?
(5)CoCl2与NaOH作用所得沉淀久置后再加浓HCl有氯气产生?


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧