题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
有Fe2+、、Fe3+、、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是氧化剂和还有Fe 2 + 、 、Fe 3 + 、 、H + 和H 2 O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是氧化剂和还原剂的物质的量之比为1∶8 B.该反应说明Fe() 2 溶液不宜加酸酸化 C.每1 mol 发生氧化反应,转移8 mol e - D.若
A.氧化剂和还原剂的物质的量之比为1∶8
B.该反应说明Fe 2 溶液不宜加酸酸化
C.每1 mol 发生氧化反应,转移8 mol e -
D.若把该反应设计为原电池,则负极反应为Fe 2 + -e - =Fe 3 +
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案


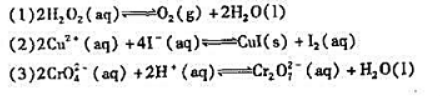
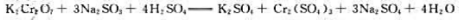 氧化剂是(),还原剂是()。
氧化剂是(),还原剂是()。 可以看出氧化还原反应的标准平衡常数与温度有关.但与反应物和生成物的浓度或分压无关。()此题为判断题(对,错)。
可以看出氧化还原反应的标准平衡常数与温度有关.但与反应物和生成物的浓度或分压无关。()此题为判断题(对,错)。 是多
是多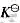 的值是()
的值是()