 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于类氢离子的能级公式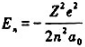 ,其中ao是().
,其中ao是().
A.玻尔半径
B.基态原子轨道半径
C.基态氢原子原子轨道半径
D.类氢离子原子轨道半径
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
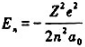 ,其中ao是().
,其中ao是().
A.玻尔半径
B.基态原子轨道半径
C.基态氢原子原子轨道半径
D.类氢离子原子轨道半径
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“对于类氢离子的能级公式,其中ao是().A.玻尔半径B.基态…”相关的问题
更多“对于类氢离子的能级公式,其中ao是().A.玻尔半径B.基态…”相关的问题
第1题
已知氨原子基态的径向波函数为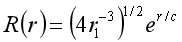 ,式中r1为玻尔第一轨道半径求电子处于玻尔第二轨道半径(r1=4r1)和玻尔第一轨道半径处的概率密度的比值。
,式中r1为玻尔第一轨道半径求电子处于玻尔第二轨道半径(r1=4r1)和玻尔第一轨道半径处的概率密度的比值。
第2题
(a)求电子处于氢原子基态时的<r>和<r2>.用玻尔(Bohr)半径表示你的结果.
(b)求电子处于氢原子基态时的<x>和<x2>.利用基态的对称性并注意到r2=x2+y2+z2.不用重新积分.
(c)对n=2,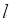 =1,m=1的态,求<x2>.注意:这个态对x,y,z不是对称的,利用x=
=1,m=1的态,求<x2>.注意:这个态对x,y,z不是对称的,利用x=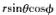 计算.
计算.
第3题
Q、R、X、Y、Z为周期表中原子序数依次递增的前四周期元素。已知: ①Q为元素周期表中原子半径最小的元素; ②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同; ③Y的基态原子的核外成对电子数是未成对电子数的3倍; ④Z有“生物金属”之称,Z 4+ 离
第4题
A.因为轨道的能量量子化,所以电子在轨道间跃迁时,发射光的频率也是不连续的
B.当原子受到激发时,核外电子获得能量,从基态跃迁到激发态而发光
C.基态氢原子的轨道半径为52.9pm
D.电子绕核在固定轨道上运动,既不放出能量也不吸收能量。
E.氢原子在通常情况下不发光,也不会发生原子自发毁灭的现象
第6题
试区别下列各术语:
(1)基态原子与激发态原子;
(2)概率与概率密度;
(3)原子轨道与电子云:
(4)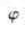 与
与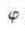 2
2
第7题
把地球一太阳引力体系类比为氢原子,
(a)势能函数是什么(替换式4.52)?(设地球质量为m,太阳质量为M)
(b)这个体系的“玻尔半径"ag为多少?给出数值结果.
(c)写出重力的“玻尔公式”,令En等同于半径为r0的行星轨道的经典能量,证明n=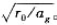 .依此估算地球的量子数n.
.依此估算地球的量子数n.
(d)假设地球跃迁到相邻的(n-1)低能级.将会释放多少能屋(以J为单位)?发射的光予波长(或许引力子)为多少?(用光年表示你的答案 这个不寻常的答案是一种巧合吗?)
第8题
第9题
A.最易失去的电子能量最高
B.同一个电子层上的不同能级上的原子轨道,能量大小相同
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
第10题
对氢原子的公式做适当修正,确定以下粒子基态的超精细分裂:(a)μ子氢电子被μ子 和电子具有相同电荷和g因子,但质量为其207倍
和电子具有相同电荷和g因子,但质量为其207倍 代替所形成的原子).(b)正电子素(质子被正电子
代替所形成的原子).(b)正电子素(质子被正电子 和电子具有相同的质量和g因子,但电荷量相反
和电子具有相同的质量和g因子,但电荷量相反 代替所形成的原子).(c)反μ子素(质子被反μ子
代替所形成的原子).(c)反μ子素(质子被反μ子 和μ子具有相同质量和g因子,但电荷量相反
和μ子具有相同质量和g因子,但电荷量相反 代替所形成的原子).在计算奇异原子的“玻尔半径”时,不要忘了应用约化质量(习题5.1).你得到的答案(4.82x10-4eV)会和实验值(8.41x10-4eV)差距很大;这个大的差异是由正负电子对湮没(e++e-→γ+γ)导致的,它贡献了(3/4)
代替所形成的原子).在计算奇异原子的“玻尔半径”时,不要忘了应用约化质量(习题5.1).你得到的答案(4.82x10-4eV)会和实验值(8.41x10-4eV)差距很大;这个大的差异是由正负电子对湮没(e++e-→γ+γ)导致的,它贡献了(3/4)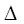 E的能量,不过这在一般的氢原子、μ子氢和反μ子素中不会发生.
E的能量,不过这在一般的氢原子、μ子氢和反μ子素中不会发生.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧