 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
关于杂化轨道理论,下列说法错误的是()。
A、杂化轨道是由不同原子的价层能量相近的原子轨道组合而成
B、有几个原子轨道参加杂化,就形成几个杂化轨道
C、杂化轨道比杂化前的原子轨道成键能力强
D、不同类型的杂化轨道间的夹角不同
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、杂化轨道是由不同原子的价层能量相近的原子轨道组合而成
B、有几个原子轨道参加杂化,就形成几个杂化轨道
C、杂化轨道比杂化前的原子轨道成键能力强
D、不同类型的杂化轨道间的夹角不同
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“关于杂化轨道理论,下列说法错误的是()。”相关的问题
更多“关于杂化轨道理论,下列说法错误的是()。”相关的问题
第1题
A、电子在整个分子范围内运动,不再属于某一特定原子
B、反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C、分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D、只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
第2题
A.只有能量相近的原子轨道才能相互杂化
B.形成的杂化轨道数等于参加杂化的原子轨道数
C.杂化轨道比原来的原子轨道更易成键
D.中心原子经杂化形成的杂化轨道均是等价的
第3题
A、中心原子采取sp3杂化轨道成键的分子,其空间构型一定是四面体
B、CH,分子中的sp3杂化轨道是由H原子的1s轨道和C原子的2p轨道组合而成
C、CH分子中的sp3杂化轨道是由C原了的1s轨道和2p轨道组合而成
D、Sp杂化轨道是由中心原子的最外层s轨道和最外层1个p轨道组合面成
第8题
A、参加杂化的各原子轨道中必须有电子存在
B、原子轨道杂化后形成的轨道数目比杂化前更多
C、原子轨道杂化后形成成键能力更强的原子轨道
D、中心原子在形成分子是所采取的的杂化方式宗师相同的
第9题
A.N2分子包含一个s键和两个π键
B.CO分子中存在配位键
C.原子形成共价键时必须遵守饱和性和方向性原则
D.sp2杂化轨道是由1s和2p轨道杂化而成
第10题
臭氧O2的键角为116.8°。若用杂化轨道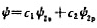 描述中心氧原子的成键轨道,试按键角与轨道成分的关系式
描述中心氧原子的成键轨道,试按键角与轨道成分的关系式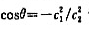 计算:
计算:
(1)成键杂化轨道ψ中系数c1和c2值;
(2)成键杂化轨道的每个原子轨道贡献的百分数。


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧