 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
20℃时,将质量为0.387g的C2H6和C4H10混合气体充入200mL的真空容器中,压力为101
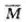 =()。
=()。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
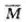 =()。
=()。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“20℃时,将质量为0.387g的C2H6和C4H10混合气体…”相关的问题
更多“20℃时,将质量为0.387g的C2H6和C4H10混合气体…”相关的问题
第1题
第2题
偶氮甲烷(CH3NNCH3)气体的分解反应
(CH3NNCH3)(g)→C2H6(g)+N2(g).
为一级反应.在287℃的真空密闭恒容容器中充入初始压力为21.332kPa的偶氮甲烷气体,反应进行1000s时测得系统的总压为22.732kPa,求速率常数k及半衰期t1/2.
第3题
第4题
温度一定密闭容器中充入压力为p的NO2(g),一定时间后下列反应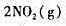
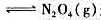 达到平衡,系统的压力为0.85p,则NO2的转化率为()
达到平衡,系统的压力为0.85p,则NO2的转化率为()
A.0.60
B.0.30
C.0.15
D.0.45
第5题
可逆反应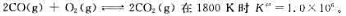 在此温度下将CO,O2和CO2充入一真空容器中,三种气体的分压分别为1kPa,10kPa和100kPa,试判断反应进行的方向。如果CO和CO2的分压不变,O2的分压为多少时,才能使反应逆向进行?
在此温度下将CO,O2和CO2充入一真空容器中,三种气体的分压分别为1kPa,10kPa和100kPa,试判断反应进行的方向。如果CO和CO2的分压不变,O2的分压为多少时,才能使反应逆向进行?
第7题
温度T时,将PCl5(g)通入一密闭容器中,发生下列反应: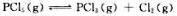 平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数
平衡时测得容器内的压力为300kPa,PCl5的平衡转化率为50%,则此温度下反应的标准平衡常数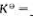 ().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
().若在此温度下,将分压均为200kPa的PCl5,PCl3和Cl2通入密闭容器中,可逆反应进行的方向是()。
第8题
.66kPa.
(1)当放人NH4CI时容器内已有压力为39.99kPa的HCl(g),求平衡时容器中的压力;
(2)容器内原有压力为6.666kPa的NH3(g),问需加多大压力的HCI,才能形成NH4CI.
(3)在520K时将0.02molNH4CI(s)和0.02molNH3引人到42.7升的抽空容器中,求平衡后各物质的量.
第9题
500℃时,可逆反应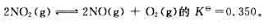 如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
第10题
6.66kPa.
(1)当放入NH4HS(s)时容器内已有39.99kPa的H2S(g),求平衡时容器中的压力;
(2)容器内原有6.666kPa的NH3(g),问H2S压力为多大时才能形成NH4HS(s)?


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧