 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
化学反应如下:(1)利用教材附录中各物质的,Δt数据,求上述反应在25℃时的(2)利用教材附录中
化学反应如下:
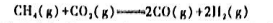
(1)利用教材附录中各物质的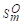 ,Δt
,Δt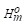 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的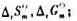
(2)利用教材附录中各物质的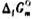 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的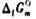 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
化学反应如下:
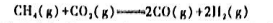
(1)利用教材附录中各物质的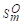 ,Δt
,Δt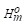 数据,求上述反应在25℃时的
数据,求上述反应在25℃时的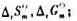
(2)利用教材附录中各物质的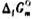 数据,计算上述及应在25℃时的
数据,计算上述及应在25℃时的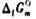 ;
;
(3)25℃,若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的ΔtSm,ΔtGm.
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“化学反应如下:(1)利用教材附录中各物质的,Δt数据,求上述…”相关的问题
更多“化学反应如下:(1)利用教材附录中各物质的,Δt数据,求上述…”相关的问题
第1题
化学反应如下:
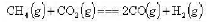
(1)利用附录中各物质的数据,求上述反应在25°C时的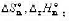
(2)利用附录中各物质的数据,计算上述反应在25°C时的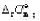
(3)25°C若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的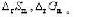
第2题
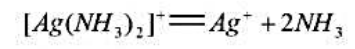
第3题
化学反应如下:CH3COOH(g)-CH4+CO2(g),298.15K各物质的数据为

求上述反应在1000K时的标准摩尔反应焓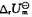 和标准摩尔反应热力学能
和标准摩尔反应热力学能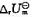 。
。
第4题
应用教材附录中有关物质的热化学数据,计算25℃时反应
2CH3OH(I)+O2(g)=HCOOCH3(I)+2H2O(I)
的标准摩尔反应焓,要求:
(1)应用25℃的标准摩尔生成焓数据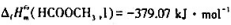 ;
;
(2)应用25℃的标准摩尔燃烧焓数据.
第5题
利用CRIME3.RAW中的数据。
(i)在教材例13.6的模型中,检验假设H0:β1=β2。(提示:定义θ1=β1-β2,并用θ1,β2和来表示β1。以此代入方程并加以整理,对θ1做t检验。)
(ii)若β1=β2,则差分方程可写成
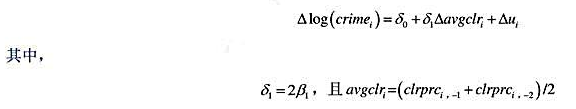
是前面两年的平均破案百分数。
(iii)估计第(ii)部分中的方程。与教材(13.22)比较调整R2。你最后会选用哪一个模型?
第6题
种以上的方法计算图3-43所示各脉冲信号的傅里叶变换,并比较三种方法.
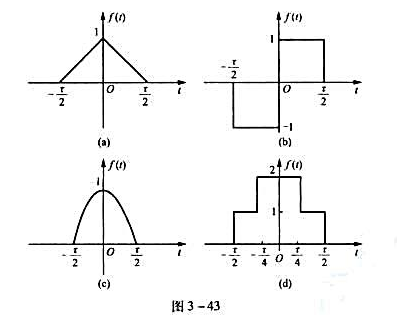
第7题
应用附录中有关物质的热化学数据,计算25℃时反应
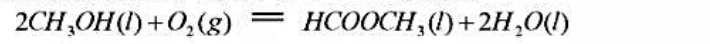
的标准摩尔反应焓,要求:(1)应用25℃的标准摩尔生成焓数据;

(2)应用25℃的标准摩尔燃烧焓数据。
第8题
已知下列化学反应于25的,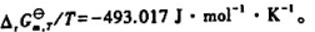

有关物质的标准摩尔吉布斯自由能函数如下表所示:

试求:(1)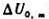 ;
;
(2)1000K时上述反应的标准平衡常数Kθ.
第9题
250K时化学反应A+2B=2C速率和浓度的关系如下:

(1)写出反应的速率方程,并指出反应指数.
(2)求该反应的速率常数.
(3)求出当c(A)=0.010mol·L-1,c(B)=0.020mol·L-1时的反应速率.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧