 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知 ,XeF4(s)的升华焓为47kJ·mol-1,试计算 。
已知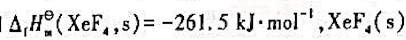 ,XeF4(s)的升华焓为47kJ·mol-1,试计算
,XeF4(s)的升华焓为47kJ·mol-1,试计算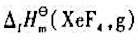 。
。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知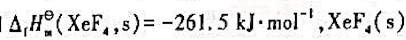 ,XeF4(s)的升华焓为47kJ·mol-1,试计算
,XeF4(s)的升华焓为47kJ·mol-1,试计算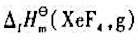 。
。
 如搜索结果不匹配,请 联系老师 获取答案
如搜索结果不匹配,请 联系老师 获取答案
 更多“已知 ,XeF4(s)的升华焓为47kJ·mol-1,试计算…”相关的问题
更多“已知 ,XeF4(s)的升华焓为47kJ·mol-1,试计算…”相关的问题
第1题
已知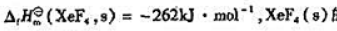 的升华焓为47kJ·mol-1,F2(g)的键解离能为158kJ·mol-1.计算:
的升华焓为47kJ·mol-1,F2(g)的键解离能为158kJ·mol-1.计算:
(1)XeF4(g)的标准摩尔生成焓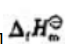 (XeF4,g);
(XeF4,g);
(2)XeF4分子中Xc-F键的键能.
第2题
为418.9kJ·mol-1,I2(g)的解离能为152.5kJ·mol-1I2(s)的标准摩尔升华焓为62.4kJ·mol-1,I(g)的电子亲和能为315.0kJ·mol-1试计算KI(s)的标准摩尔生成焓。
第3题
已知钡的升华焓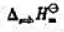 =180.0kJ·mol-1,第一、第二电离能分别为
=180.0kJ·mol-1,第一、第二电离能分别为
507.94kJ·mol-1和971.44kJ·mol-1,Ba2+(aq)的标准摩尔生成烩的相对值(Ba2+,q)=-537.64kJ.mol-1.试用热力学循环计算;(1)Ba2+(g)的标准摩尔生成焓ΔlHθm(Ba2+,g);(2)Ba2+(g)的水合焓ΔhHθm(Ba2+,g).
第4题
已知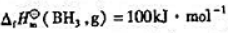 试根据书末附表中的有关热力学数据计算:
试根据书末附表中的有关热力学数据计算:
(1)B-H键键焓;(2)乙硼烷中BBH键的键焓.
第5题
实验测得固态和液态氢醌的蒸气压数据如下:

(1) 计算氢醌的升华焰,蒸发焓和熔化焓;
(2)确定三相点温度及压力.
假设相变焓为常数.
第8题
已知298.15K时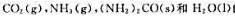 的标准摩尔生成焓和标准摩尔熵如下表所示:
的标准摩尔生成焓和标准摩尔熵如下表所示:

试通过计算判断下列反应
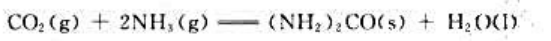
在298.15K、标准状态下能否自发进行。上述反应在标准状态下自发进行的最高温度是多少?
第9题
298K时,下列电池的电动势为1.228V:
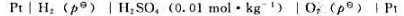
已知H2O(I)的标准生成焓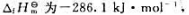 试求:
试求:
(1)该电池的温度系数:
(2)该电池在273K时的电动势.设反应焓在273~298K间为常数.


为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!

 微信搜一搜
微信搜一搜
 上学吧
上学吧



 微信搜一搜
微信搜一搜
 上学吧
上学吧